La terapia con cellule T CAR, un approccio innovativo al trattamento di alcuni tipi di cancro, si basa sulla modifica genetica delle cellule immunitarie del paziente per colpire e distruggere le cellule tumorali. Questo complesso processo richiede procedure di laboratorio altamente specializzate ed è essenziale dare priorità alla sicurezza delle cellule modificate, del paziente e degli operatori sanitari coinvolti.
Questo articolo approfondisce il processo di modificazione genetica delle cellule CAR T, il ruolo cruciale del controllo della contaminazione e il ruolo fondamentale dei dispositivi di protezione individuale (DPI) nel mantenere un ambiente sicuro.
Il processo di modifica genetica delle cellule CAR T
1. Raccolta di cellule T
- Le cellule T vengono raccolte tramite leucaferesi, un processo simile alla donazione di sangue.
- La leucaferesi isola le cellule T dagli altri componenti del sangue.
- Le condizioni di sterilità impediscono la contaminazione in questa fase critica.
2. Isolamento e attivazione
- Le cellule T vengono isolate e attivate in un ambiente di laboratorio controllato.
- Le cellule vengono coltivate e preparate per la modifica.
3. Modifica genetica
- Viene introdotto un gene Chimeric Antigen Receptor (CAR) per consentire di colpire il cancro.
- Per veicolare il gene in modo sicuro si utilizzano vettori lentivirali o retrovirali.
- Il controllo della contaminazione garantisce l'integrità delle modifiche.
4. Espansione
- Le cellule T modificate vengono espanse a livelli terapeutici.
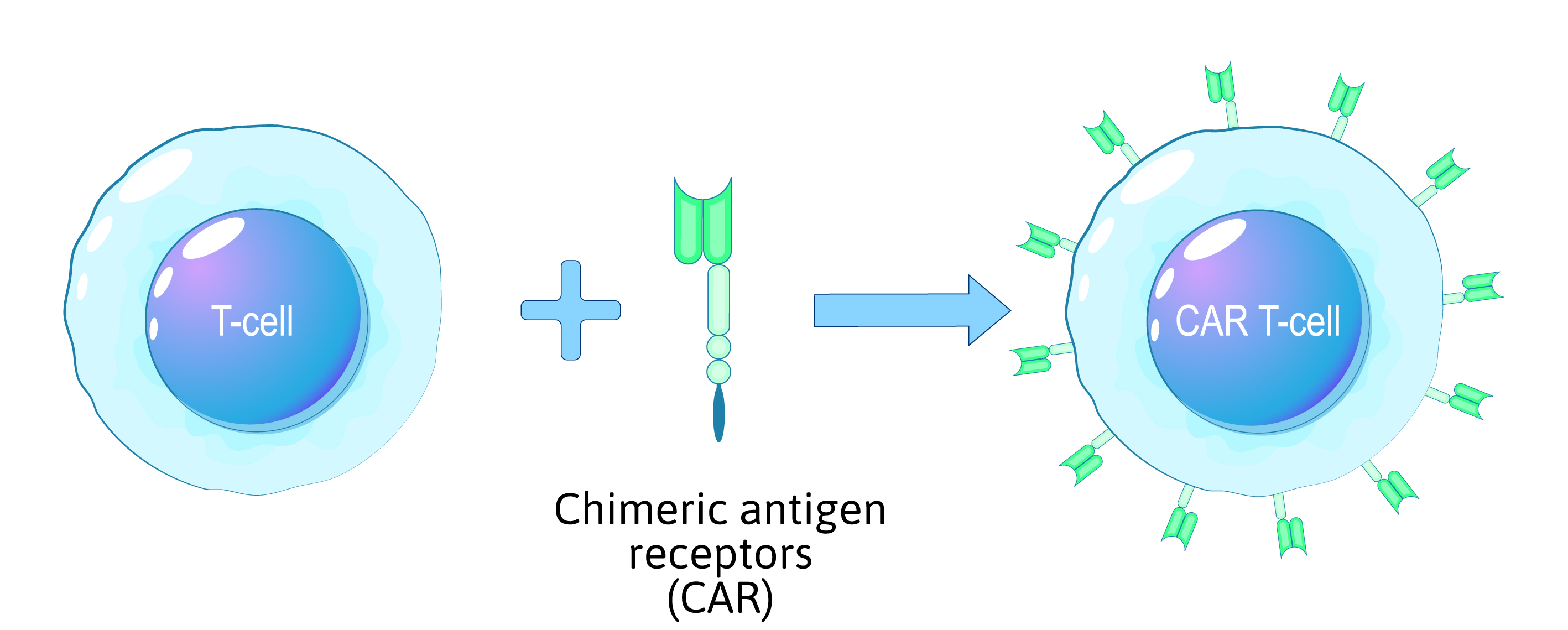 Figura 1: Panoramica del processo di riprogrammazione delle cellule T CAR.
Figura 1: Panoramica del processo di riprogrammazione delle cellule T CAR.
5. Controllo qualità
- Le cellule vengono testate per verificarne la purezza, la vitalità e l'efficacia.
- Solo le cellule di migliore qualità passano alla fase successiva.
6. Infusione nel paziente
- Le cellule T CAR modificate vengono infuse nel paziente.
- Questo segna l'inizio di una risposta immunitaria mirata contro il cancro.
Misure di controllo della contaminazione
Un efficace controllo della contaminazione è indispensabile durante tutto il processo di modificazione genetica delle cellule CAR T per mantenere l'integrità della terapia e garantire la sicurezza dei pazienti e del personale di laboratorio. Le principali misure di controllo della contaminazione includono:
1. Tecniche sterili:
Il personale di laboratorio deve attenersi scrupolosamente alle tecniche sterili, tra cui lavaggio delle mani, camice e guanti, per garantire la sterilità di tutte le attrezzature e dei materiali utilizzati.
2. Cabine di sicurezza biologica (BSC):
La modificazione genetica delle cellule avviene all'interno di cabine di sicurezza biologica di Classe II, che forniscono un ambiente controllato e sterile. Questi armadi contribuiscono a contenere i potenziali contaminanti e a proteggere i lavoratori del laboratorio.
3. Strutture per camere bianche:
La produzione di cellule T CAR avviene spesso in strutture di classe ISO, progettate specificamente per mantenere elevati livelli di pulizia e controllare la contaminazione da particolato.
4. Barriere di isolamento:
Le barriere di isolamento fisico, come le cappe a flusso laminare e i sistemi chiusi, sono utilizzate per prevenire la contaminazione durante i processi di manipolazione e coltura delle cellule.
5. Monitoraggio di routine:
Il monitoraggio regolare degli ambienti di laboratorio per la qualità dell'aria, la contaminazione delle superfici e la presenza di microbi è essenziale per identificare e affrontare tempestivamente le potenziali fonti di contaminazione. Tra gli strumenti di monitoraggio più comuni vi sono i contatori di particelle e i campionatori microbici.
6. Smaltimento dei rifiuti:
Lo smaltimento corretto dei materiali di scarto, comprese le attrezzature potenzialmente contaminate e i rifiuti biologici, è fondamentale per prevenire la contaminazione. Lo smaltimento dei materiali contaminati, compresi quelli taglienti, è fondamentale per prevenire qualsiasi esposizione accidentale del personale.


