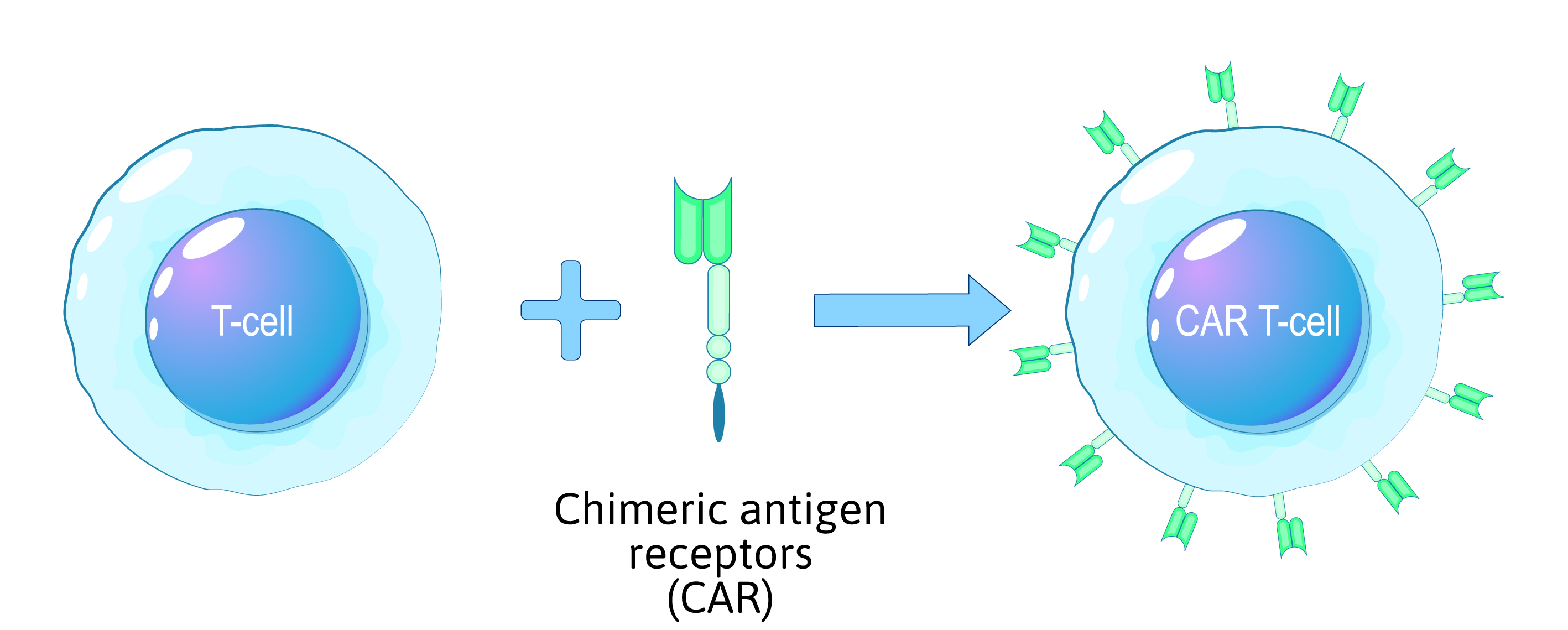
La thérapie CAR T, une approche innovante pour traiter certains types de cancer, repose sur la modification génétique des cellules immunitaires d'un patient pour cibler et détruire les cellules cancéreuses. Ce processus complexe nécessite des procédures de laboratoire hautement spécialisées, et il est essentiel de donner la priorité à la sécurité des cellules modifiées, du patient et des professionnels de la santé impliqués.
Cet article examine le processus de modification génétique des cellules CAR T, le rôle crucial que joue le contrôle de la contamination et le rôle essentiel de l'équipement de protection individuelle (EPI) dans le maintien d'un environnement sûr.
Le processus de modification génétique des cellules CAR T
-
Collecte de cellules T :
- Le processus de thérapie CAR T commence par la collecte des cellules T d'un patient par leucaphérèse, une procédure similaire au don de sang.
- La leucaphérèse sépare les cellules T des autres composants sanguins, ce qui garantit une concentration élevée des cellules cibles.
- Il est essentiel de garantir un environnement de prélèvement propre et stérile pour éviter toute contamination, car tout compromis au début du processus peut avoir un impact sur l'efficacité de la thérapie.
-
Isolement et activation:
- Une fois prélevées, les cellules T sont isolées et activées en laboratoire. Ils sont ensuite cultivés pour s'assurer qu'ils sont dans un état actif et prêts à être modifiés.
- Une fois prélevées, les cellules T sont isolées et activées en laboratoire. Ils sont ensuite cultivés pour s'assurer qu'ils sont dans un état actif et prêts à être modifiés.
-
Modification génétique:
- La modification génétique est une étape critique dans le processus des cellules CAR T. Les scientifiques introduisent une nouvelle séquence génétique dans les cellules T pour leur permettre d'exprimer le récepteur d'antigène chimérique (CAR).
- Ce CAR est conçu pour reconnaître des antigènes spécifiques présents à la surface des cellules cancéreuses.
- Des vecteurs lentiviraux ou rétroviraux sont généralement utilisés pour introduire le gène CAR dans le génome des cellules T. Un contrôle strict de la contamination garantit l'intégrité du processus de modification génétique.
-
Expansion:
- Après modification génétique, les cellules CAR T sont développées en culture pour créer une plus grande population de ces cellules immunitaires spécialisées. Cette étape permet de s'assurer qu'il y a suffisamment de cellules CAR T pour mettre en place une réponse immunitaire efficace.
Figure 1 : Aperçu du processus de reprogrammation des cellules T CAR à l'aide de récepteurs antigéniques chimériques (CAR).
- Après modification génétique, les cellules CAR T sont développées en culture pour créer une plus grande population de ces cellules immunitaires spécialisées. Cette étape permet de s'assurer qu'il y a suffisamment de cellules CAR T pour mettre en place une réponse immunitaire efficace.
-
Contrôle de la qualité:
- Des mesures rigoureuses de contrôle de la qualité sont en place pour garantir que les cellules T modifiées sont sûres et efficaces. Il s'agit notamment d'évaluer la pureté, la viabilité et la fonctionnalité des cellules CAR T.
- Des mesures rigoureuses de contrôle de la qualité sont en place pour garantir que les cellules T modifiées sont sûres et efficaces. Il s'agit notamment d'évaluer la pureté, la viabilité et la fonctionnalité des cellules CAR T.
-
Infusion dans le patient:
- L'étape finale consiste à réinjecter les cellules CAR T modifiées dans la circulation sanguine du patient. Cette perfusion marque le début de la phase thérapeutique, au cours de laquelle les cellules CAR T reconnaissent et attaquent les cellules cancéreuses avec l'antigène ciblé.
- L'étape finale consiste à réinjecter les cellules CAR T modifiées dans la circulation sanguine du patient. Cette perfusion marque le début de la phase thérapeutique, au cours de laquelle les cellules CAR T reconnaissent et attaquent les cellules cancéreuses avec l'antigène ciblé.
Mesures de contrôle de la contamination
Un contrôle efficace de la contamination est impératif tout au long du processus de modification génétique des cellules CAR T afin de maintenir l'intégrité de la thérapie et de garantir la sécurité des patients et du personnel de laboratoire. Les principales mesures de contrôle de la contamination sont les suivantes
-
Techniques stériles: Le personnel de laboratoire doit respecter strictement les techniques stériles, y compris le lavage des mains, le port de la blouse et des gants, afin de s'assurer que tous les équipements et matériels utilisés sont stériles.
-
Cabinets de sécurité biologique (BSC): La modification génétique des cellules a lieu dans des enceintes de sécurité biologique de classe II, qui offrent un environnement contrôlé et stérile. Ces armoires permettent de contenir les contaminants potentiels et de protéger le personnel de laboratoire.
-
Installations de salle blanche: La production de cellules CAR T a souvent lieu dans des salles blanches de classe ISO, spécialement conçues pour maintenir des niveaux élevés de propreté et contrôler la contamination particulaire.
-
Barrières d'isolement: Les barrières d'isolement physique, telles que les hottes à flux laminaire et les systèmes fermés, sont utilisées pour prévenir la contamination pendant les processus de manipulation et de culture des cellules.
-
Surveillance de routine: Il est essentiel de contrôler régulièrement la qualité de l'air, la contamination des surfaces et la présence microbienne dans les laboratoires afin d'identifier les sources potentielles de contamination et d'y remédier rapidement. Les outils de surveillance les plus courants sont les compteurs de particules et les échantillonneurs microbiens.
-
Élimination des déchets : il est essentiel d'éliminer correctement les déchets, y compris les équipements potentiellement contaminés et les déchets biologiques, afin d'éviter toute contamination. L'élimination du matériel contaminé, y compris les objets tranchants, est essentielle pour éviter toute exposition accidentelle du personnel.