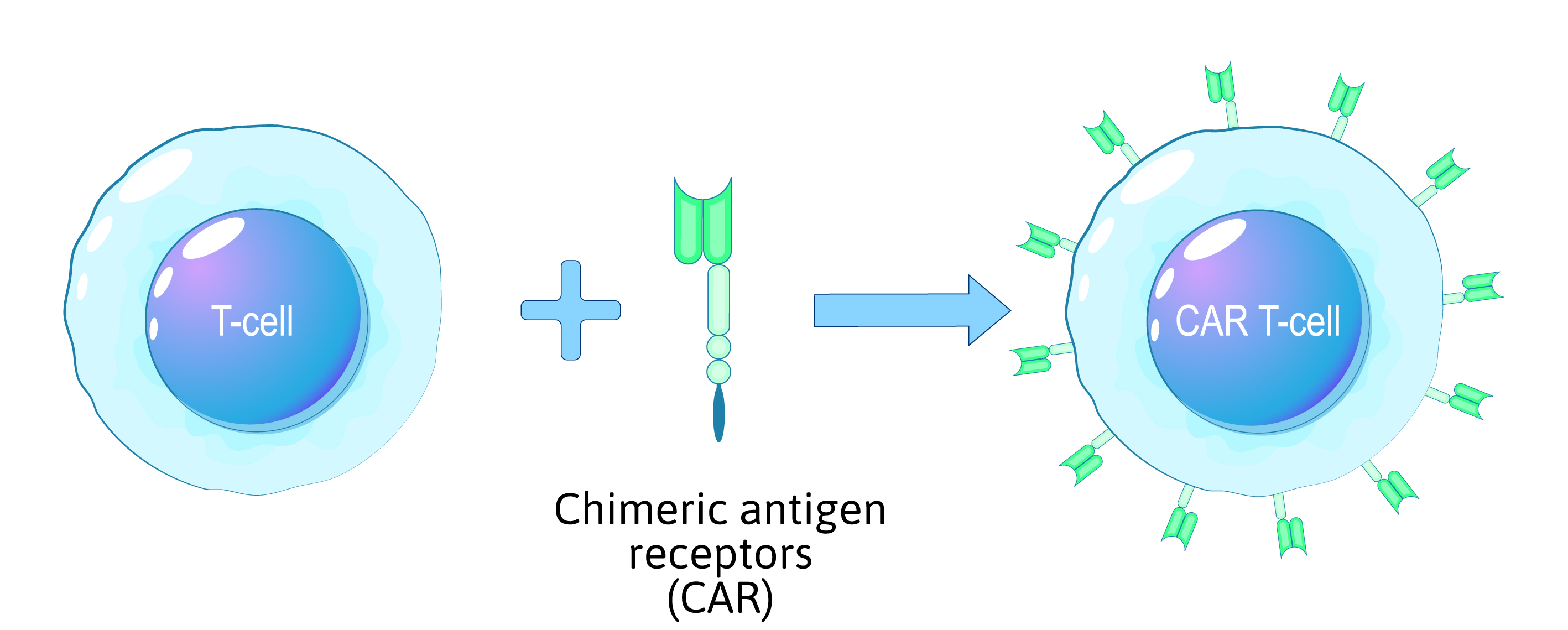
A terapia com células T CAR, uma abordagem inovadora para o tratamento de certos tipos de cancro, baseia-se na modificação genética das células imunitárias de um doente para atingir e destruir as células cancerígenas. Este processo complexo requer procedimentos laboratoriais altamente especializados, sendo essencial dar prioridade à segurança das células modificadas, do doente e dos profissionais de saúde envolvidos.
Este artigo analisa o processo de modificação genética das células CAR T, o papel crucial que o controlo da contaminação desempenha e o papel crítico do Equipamento de Proteção Individual (EPI) na manutenção de um ambiente seguro.
O processo de modificação genética das células T CAR
-
Recolha de células T:
- O processo de terapia com células T CAR começa com a recolha das células T de um doente através de leucaférese, um procedimento semelhante à dádiva de sangue.
- A leucaférese separa as células T de outros componentes do sangue, assegurando uma elevada concentração das células-alvo.
- Garantir um ambiente de colheita limpo e estéril é essencial para evitar a contaminação, uma vez que qualquer compromisso no início do processo pode afetar a eficácia da terapia.
-
Isolamento e ativação:
- Uma vez recolhidas, as células T são isoladas e activadas em laboratório. São depois cultivadas para garantir que estão num estado ativo e prontas para serem modificadas.
- Uma vez recolhidas, as células T são isoladas e activadas em laboratório. São depois cultivadas para garantir que estão num estado ativo e prontas para serem modificadas.
-
Modificação genética:
- A modificação genética é um passo crítico no processo das células T CAR. Os cientistas introduzem uma nova sequência genética nas células T para que estas possam expressar o Recetor de Antigénio Quimérico (CAR).
- Este CAR foi concebido para reconhecer antigénios específicos que se encontram na superfície das células cancerígenas.
- Os vectores lentivirais ou retrovirais são normalmente utilizados para introduzir o gene CAR no genoma das células T. Um controlo rigoroso da contaminação garante a integridade do processo de modificação genética.
-
Expansão:
- Após a modificação genética, as células CAR T são expandidas em cultura para criar uma população maior destas células imunitárias especializadas. Este passo assegura que existem células CAR T suficientes para montar uma resposta imunitária eficaz.
Figura 1: Visão geral do processo de reprogramação das células T CAR utilizando receptores de antigénios quiméricos (CAR).
- Após a modificação genética, as células CAR T são expandidas em cultura para criar uma população maior destas células imunitárias especializadas. Este passo assegura que existem células CAR T suficientes para montar uma resposta imunitária eficaz.
-
Controlo de qualidade:
- Estão em vigor medidas rigorosas de controlo de qualidade para garantir que as células T modificadas são seguras e eficazes. Isto inclui a avaliação da pureza, viabilidade e funcionalidade das células CAR T.
- Estão em vigor medidas rigorosas de controlo de qualidade para garantir que as células T modificadas são seguras e eficazes. Isto inclui a avaliação da pureza, viabilidade e funcionalidade das células CAR T.
-
Infusão no paciente:
- O passo final consiste em infundir as células CAR T modificadas de novo na corrente sanguínea do doente. Esta infusão marca o início da fase terapêutica, em que as células CAR T reconhecem e atacam as células cancerígenas com o antigénio visado.
- O passo final consiste em infundir as células CAR T modificadas de novo na corrente sanguínea do doente. Esta infusão marca o início da fase terapêutica, em que as células CAR T reconhecem e atacam as células cancerígenas com o antigénio visado.
Medidas de controlo da contaminação
É imperativo um controlo eficaz da contaminação durante todo o processo de modificação genética das células CAR T para manter a integridade da terapia e garantir a segurança dos doentes e do pessoal do laboratório. As principais medidas de controlo da contaminação incluem:
-
Técnicas estéreis: O pessoal do laboratório deve respeitar rigorosamente as técnicas de esterilização, incluindo a lavagem das mãos, a utilização de batas e de luvas, para garantir que todo o equipamento e materiais utilizados são estéreis.
-
Armários de segurança biológica (BSC): A modificação genética das células é efectuada em armários de segurança biológica de classe II, que proporcionam um ambiente controlado e estéril. Estes armários ajudam a conter potenciais contaminantes e a proteger os trabalhadores do laboratório.
-
Instalações para salas limpas: A produção de células T CAR ocorre frequentemente em instalações de salas limpas de classe ISO, que são especificamente concebidas para manter elevados níveis de limpeza e controlar a contaminação por partículas.
-
Barreiras de isolamento: As barreiras de isolamento físico, tais como campânulas de fluxo laminar e sistemas fechados, são utilizadas para evitar a contaminação durante os processos de manipulação e cultura de células.
-
Monitorização de rotina: A monitorização regular dos ambientes laboratoriais no que respeita à qualidade do ar, à contaminação da superfície e à presença microbiana é essencial para identificar e tratar prontamente as potenciais fontes de contaminação. As ferramentas comuns de monitorização incluem contadores de partículas e amostradores microbianos.
-
Eliminação de resíduos: A eliminação adequada de resíduos, incluindo equipamento potencialmente contaminado e resíduos biológicos, é crucial para evitar a contaminação. A eliminação de materiais contaminados, incluindo material cortante, é vital para evitar qualquer exposição acidental do pessoal.